पहले और दूसरे क्रम की प्रतिक्रियाओं के बीच महत्वपूर्ण अंतर यह है कि पहले क्रम की प्रतिक्रियाओं की दर दर समीकरण में अभिकारक एकाग्रता की पहली शक्ति पर निर्भर करती है जबकि दूसरे क्रम की प्रतिक्रियाओं की दर एकाग्रता की दूसरी शक्ति पर निर्भर करती है दर समीकरण में पद।
एक प्रतिक्रिया का क्रम उन शक्तियों का योग है जिनसे अभिकारक सांद्रता दर कानून समीकरण में बढ़ जाती है। इस परिभाषा के अनुसार प्रतिक्रियाओं के कई रूप हैं; शून्य कोटि की अभिक्रियाएँ (ये अभिक्रियाएँ अभिकारकों की सांद्रता पर निर्भर नहीं करती हैं), प्रथम कोटि की अभिक्रियाएँ तथा द्वितीय कोटि की अभिक्रियाएँ।
प्रथम आदेश प्रतिक्रिया क्या हैं?
प्रथम कोटि की अभिक्रियाएँ रासायनिक अभिक्रियाएँ होती हैं जिनमें अभिक्रिया की दर अभिक्रिया में शामिल किसी एक अभिकारक की मोलर सांद्रता पर निर्भर करती है। इसलिए, प्रतिक्रिया के क्रम के लिए उपरोक्त परिभाषा के अनुसार, दर कानून समीकरण में अभिकारक सांद्रता को बढ़ाने वाली शक्तियों का योग हमेशा 1 होगा। इन प्रतिक्रियाओं में भाग लेने वाला एक एकल अभिकारक हो सकता है। तब उस अभिकारक की सांद्रता अभिक्रिया की दर निर्धारित करती है। लेकिन कभी-कभी, एक से अधिक अभिकारक होते हैं जो इन अभिक्रियाओं में भाग लेते हैं, तो इनमें से कोई एक अभिकारक प्रतिक्रिया की दर निर्धारित करेगा।
इस अवधारणा को समझने के लिए एक उदाहरण पर विचार करते हैं। N2O5 की अपघटन प्रतिक्रिया में, यह NO2 और O बनाता है। 2 गैसें उत्पादों के रूप में। चूँकि इसमें केवल एक अभिकारक होता है, इसलिए हम अभिक्रिया और दर समीकरण इस प्रकार लिख सकते हैं।
2N2O5(g) → 4NO2(g) + O 2(जी)
दर=कश्मीर[एन2ओ5(जी)]एम
यहाँ k इस प्रतिक्रिया के लिए स्थिर दर है और m प्रतिक्रिया का क्रम है। इसलिए, प्रायोगिक निर्धारणों से, m का मान 1 है। इस प्रकार, यह एक प्रथम कोटि की प्रतिक्रिया है।
दूसरे क्रम की प्रतिक्रियाएं क्या हैं?
द्वितीय क्रम की प्रतिक्रियाएं रासायनिक प्रतिक्रियाएं होती हैं जिनमें प्रतिक्रिया की दर दो अभिकारकों की दाढ़ की एकाग्रता या प्रतिक्रिया में शामिल एक अभिकारक की दूसरी शक्ति पर निर्भर करती है। इसलिए, प्रतिक्रिया के क्रम के लिए उपरोक्त परिभाषा के अनुसार, दर कानून समीकरण में अभिकारक सांद्रता को बढ़ाने वाली शक्तियों का योग हमेशा 2 होगा। यदि दो अभिकारक हैं, तो प्रतिक्रिया की दर पहली शक्ति पर निर्भर करेगी। प्रत्येक अभिकारक की सांद्रता का।
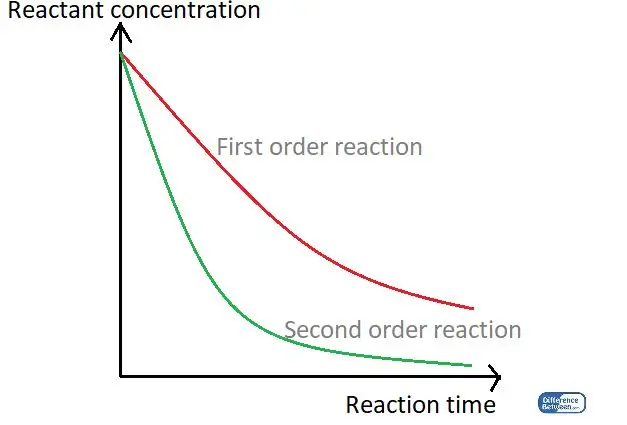
चित्र 01: प्रतिक्रिया समय और अभिकारक एकाग्रता का उपयोग करके दो प्रकार की प्रतिक्रिया के क्रम की तुलना करने वाला एक ग्राफ।
यदि हम किसी अभिकारक की सांद्रता को 2 गुना बढ़ा दें (यदि दर समीकरण में दो अभिकारक हों), तो प्रतिक्रिया की दर 4 गुना बढ़ जाती है। उदाहरण के लिए, आइए निम्नलिखित प्रतिक्रिया पर विचार करें।
2ए → पी
यहाँ A अभिकारक है और P उत्पाद है। फिर यदि यह द्वितीय कोटि की अभिक्रिया है, तो इस अभिक्रिया के लिए दर समीकरण इस प्रकार है।
दर=कश्मीर[ए]2
लेकिन दो अलग-अलग अभिकारकों के साथ प्रतिक्रिया के लिए जैसे कि;
ए + बी → पी
दर=कश्मीर[ए]1[बी]1
पहले और दूसरे क्रम की प्रतिक्रियाओं में क्या अंतर है?
प्रथम कोटि की अभिक्रियाएँ रासायनिक अभिक्रियाएँ होती हैं जिनमें अभिक्रिया की दर अभिक्रिया में शामिल किसी एक अभिकारक की मोलर सांद्रता पर निर्भर करती है।इसलिए, यदि हम अभिकारक की सांद्रता को 2 गुना बढ़ा दें, तो प्रतिक्रिया की दर 2 गुना बढ़ जाती है। दूसरे क्रम की प्रतिक्रियाएं रासायनिक प्रतिक्रियाएं होती हैं जिनमें प्रतिक्रिया की दर दो अभिकारकों की दाढ़ की एकाग्रता या प्रतिक्रिया में शामिल एक अभिकारक की दूसरी शक्ति पर निर्भर करती है। इसलिए, यदि हम अभिकारक की सांद्रता को 2 गुना बढ़ा दें, तो प्रतिक्रिया की दर 4 गुना बढ़ जाती है। नीचे दिया गया इन्फोग्राफिक पहले और दूसरे क्रम की प्रतिक्रियाओं के बीच अंतर को सारणीबद्ध रूप में प्रस्तुत करता है।

सारांश - पहले बनाम दूसरे क्रम की प्रतिक्रियाएं
प्रतिक्रिया के क्रम के अनुसार तीन प्रमुख प्रकार की प्रतिक्रियाएं होती हैं; शून्य कोटि, प्रथम कोटि तथा द्वितीय कोटि की अभिक्रियाएँ। पहले और दूसरे क्रम की प्रतिक्रियाओं के बीच महत्वपूर्ण अंतर यह है कि पहले क्रम की प्रतिक्रिया की दर दर समीकरण में अभिकारक एकाग्रता की पहली शक्ति पर निर्भर करती है जबकि दूसरे क्रम की प्रतिक्रिया की दर एकाग्रता अवधि की दूसरी शक्ति पर निर्भर करती है दर समीकरण।







