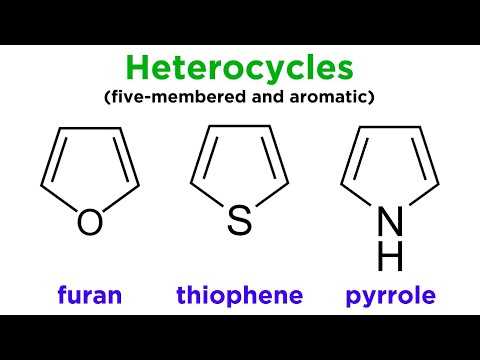
पाइरोल फुरान और थियोफीन के बीच महत्वपूर्ण अंतर यह है कि पाइरोल में पांच-सदस्यीय कार्बन रिंग में एक -NH समूह होता है और फुरान में पांच-सदस्यीय कार्बन रिंग में एक ऑक्सीजन परमाणु होता है, जबकि थियोफीन में पांच-सदस्यीय सल्फर परमाणु होता है। -सदस्य कार्बन रिंग।
पाइरोल फुरान और थियोफीन कार्बनिक यौगिक हैं। ये पांच-सदस्यीय वलय संरचनाएं हैं जिनमें एक कार्बन परमाणु को एक अलग समूह जैसे कि एक अमीन समूह, एक ऑक्सीजन परमाणु या एक सल्फर परमाणु से बदल दिया जाता है।
पाइरोल क्या है?
पाइरोल पांच सदस्यीय वलय है जिसका रासायनिक सूत्र C4H4NH है।यह एक विषमचक्रीय यौगिक है जिसमें एक नाइट्रोजन परमाणु चार अन्य कार्बन परमाणुओं के साथ वलय संरचना के निर्माण में योगदान देता है। हम कमरे के तापमान पर पायरोल को एक वाष्पशील और रंगहीन तरल के रूप में देख सकते हैं। हालांकि, सामान्य हवा के संपर्क में आने पर, तरल आसानी से काला हो जाता है। इसलिए, हमें उपयोग करने से पहले इसे शुद्ध करने की आवश्यकता है। शुद्धिकरण उपयोग से तुरंत पहले आसवन के माध्यम से किया जा सकता है। इसके अलावा, इस तरल में अखरोट की गंध होती है।

चित्र 01: पाइरोल की संरचना
फुरान और थियोफीन जैसे कुछ अन्य पांच-सदस्यीय हेट्रोसायक्लिक रिंगों के विपरीत, पायरोल में एक द्विध्रुवीय होता है जिसमें अंगूठी का सकारात्मक पक्ष हेटेरोएटम पर होता है (-एनएच समूह सकारात्मक चार्ज करता है)। पायरोल एक कमजोर क्षारकीय यौगिक है।
इसके अलावा, यह यौगिक प्रकृति में डेरिवेटिव के रूप में होता है।उदाहरण के लिए, विटामिन बी 12, पित्त वर्णक जैसे बिलीरुबिन, पोर्फिरिन, आदि पाइरोल डेरिवेटिव हैं। हालाँकि, यह यौगिक थोड़ा विषैला होता है। औद्योगिक पैमाने में, हम अमोनिया के साथ फुरान के उपचार के माध्यम से पाइरोल को संश्लेषित कर सकते हैं। लेकिन, इस प्रतिक्रिया के लिए एक ठोस उत्प्रेरक की भी आवश्यकता होती है।
फुरान क्या है?
फुरान एक पांच-सदस्यीय वलय संरचना है जिसमें वलय के एक भाग के रूप में ऑक्सीजन परमाणु होता है। इसका मतलब है, एक ऑक्सीजन परमाणु, चार कार्बन परमाणुओं के साथ, फुरान की पांच-सदस्यीय वलय बनाता है। इसे एरोमैटिक हेटरोसायक्लिक रिंग का नाम दिया गया है। कमरे के तापमान पर, यह यौगिक रंगहीन और अत्यधिक वाष्पशील तरल के रूप में बाहर निकलता है। साथ ही यह द्रव ज्वलनशील भी होता है। फुरान का क्वथनांक कमरे के तापमान के बहुत करीब होता है। इसके अलावा, इसमें एक मजबूत, ईथर जैसी गंध है। विषाक्तता पर विचार करते समय, फुरान अत्यधिक विषैला होता है और मानव में कार्सिनोजेनिक हो सकता है।

चित्र 02: फुरान की संरचना
इसके अलावा, फुरान की सुगंध ऑक्सीजन परमाणु के एकाकी इलेक्ट्रॉन जोड़े के वलय में निरूपित होने के कारण होती है। इसके अलावा, यह यौगिक इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं में बेंजीन की तुलना में काफी अधिक प्रतिक्रियाशील है। यह ऑक्सीजन परमाणु के इलेक्ट्रॉन-दान करने वाले व्यवहार के कारण है।
औद्योगिक पैमाने में, हम पैलेडियम उत्प्रेरक की उपस्थिति में फरफुरल के डीकार्बोनाइलेशन के माध्यम से फ्यूरान का उत्पादन कर सकते हैं। या फिर, हम एक अन्य विधि का उपयोग कर सकते हैं जिसमें कॉपर उत्प्रेरक की उपस्थिति में 1, 3-ब्यूटाडाइन का ऑक्सीकरण किया जाता है।
थियोफीन क्या है?
थियोफीन एक पांच-सदस्यीय वलय संरचना है जिसमें एक सल्फर परमाणु और रिंग में चार कार्बन परमाणु होते हैं। इसलिए, यह एक सुगन्धित, विषमचक्रीय वलय है। संरचना का रासायनिक सूत्र C4H4S है। यह एक रंगहीन तरल है जिसमें बेंजीन जैसी गंध होती है।थियोफीन और बेंजीन के बीच कई अन्य समानताएं हैं जैसे कि प्रतिक्रियाशीलता। सल्फोनेशन के प्रति थियोफीन की उच्च प्रतिक्रियाशीलता के आधार पर हम थायोफीन को बेंजीन से अलग कर सकते हैं।

चित्र 03: थियोफीन की संरचना
थियोफीन के उत्पादन पर विचार करते समय, विश्वव्यापी उत्पादन में कार्बन डाइसल्फ़ाइड और ब्यूटेनॉल की वाष्प चरण प्रतिक्रिया शामिल होती है। साथ ही, इस प्रतिक्रिया के लिए ऑक्सीजन उत्प्रेरक और उच्च तापमान की आवश्यकता होती है।
पाइरोल फुरान और थियोफीन में क्या अंतर है?
पाइरोल, फुरान और थियोफीन कार्बनिक यौगिक हैं। ये पांच-सदस्यीय वलय संरचनाएं हैं जिनमें एक कार्बन परमाणु को एक अलग समूह जैसे कि एक अमीन समूह, एक ऑक्सीजन परमाणु या एक सल्फर परमाणु से बदल दिया जाता है। इसलिए, पाइरोल फुरान और थियोफीन के बीच महत्वपूर्ण अंतर यह है कि पाइरोल में पांच-सदस्यीय कार्बन रिंग में एक -NH समूह होता है और फ्यूरान में पांच-सदस्यीय कार्बन रिंग में एक ऑक्सीजन परमाणु होता है, जबकि थियोफीन में पांच-सदस्यीय में एक सल्फर परमाणु होता है। कार्बन की अंगूठी।
नीचे इन्फोग्राफिक पाइरोल फुरान और थियोफीन के बीच अंतर को सारांशित करता है।

सारांश - पाइरोल बनाम फुरान बनाम थियोफीन
पाइरोल, फुरान और थियोफीन कार्बनिक यौगिक हैं। ये पांच-सदस्यीय वलय संरचनाएं हैं जिनमें एक कार्बन परमाणु को एक अलग समूह जैसे कि एक अमीन समूह, एक ऑक्सीजन परमाणु या एक सल्फर परमाणु से बदल दिया जाता है। इसलिए, पाइरोल, फुरान और थियोफीन के बीच महत्वपूर्ण अंतर यह है कि पाइरोल में पांच-सदस्यीय कार्बन रिंग में एक -NH समूह होता है और फ्यूरान में पांच-सदस्यीय कार्बन रिंग में एक ऑक्सीजन परमाणु होता है, जबकि थियोफीन में एक सल्फर परमाणु होता है। सदस्य कार्बन रिंग।