पीएक्स पाय और पीजेड ऑर्बिटल्स के बीच महत्वपूर्ण अंतर यह है कि पीएक्स ऑर्बिटल में एक्स-एक्सिस के साथ दो लोब उन्मुख होते हैं और पी ऑर्बिटल में दो लोब होते हैं जो वाई-अक्ष के साथ उन्मुख होते हैं, जबकि पीजेड ऑर्बिटल में दो लोब उन्मुख होते हैं। z-अक्ष के अनुदिश। इसलिए, Px Py और Pz ऑर्बिटल्स के बीच अंतर अंतरिक्ष में उनके उन्मुखीकरण से उत्पन्न होता है।
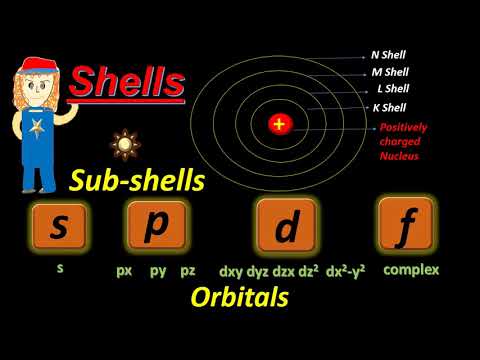
परमाणु कक्षक एक परमाणु नाभिक के चारों ओर का क्षेत्र होता है, जिसमें इलेक्ट्रॉन मिलने की संभावना सबसे अधिक होती है। परमाणु के कक्षक या तो s कक्षीय, p कक्षीय, d कक्षीय या f कक्षीय हो सकते हैं। इसके अलावा, तीन पी ऑर्बिटल्स हैं; वे Px, Py और Pz कक्षक हैं।

पीएक्स ऑर्बिटल क्या है?
Px कक्षीय तीन p कक्षकों में से एक है और x-अक्ष के अनुदिश उन्मुख है। इसके अलावा, इस कक्षीय में दो पालियाँ होती हैं और इसमें डम्बल का आकार होता है। क्वांटम संख्याएँ संख्याओं का एक समूह है जो परमाणु कक्षाओं को नाम देने में मदद करती है। यह प्रणाली एक विशेष परमाणु कक्षीय को एक अनूठा नाम देती है।

चित्र 1: विभिन्न पी ऑर्बिटल्स और उनकी ओरिएंटेशन
क्वांटम नंबर:
- सिद्धांत क्वांटम संख्या (एन) इलेक्ट्रॉन खोल का वर्णन करता है। उदाहरण: n=1, 2, 3…
- अजीमुथल क्वांटम संख्या या कोणीय गति क्वांटम संख्या (एल) उपकोशों की व्याख्या करती है। उदाहरण: एल=0, 1, 2…
- चुंबकीय क्वांटम संख्या (एम) एक इलेक्ट्रॉन की अद्वितीय क्वांटम स्थिति को इंगित करती है। उदाहरण: एम=…-2, -1, 0, +1, +2…
- स्पिन क्वांटम संख्या (एस) एक इलेक्ट्रॉन के स्पिन का वर्णन करती है। उदाहरण: एस=±
Px कक्षीय पर विचार करते समय, क्वांटम संकेतन इस प्रकार है।
- जब n=1, कोई P ऑर्बिटल्स नहीं होते हैं।
- जब n > 2, और l=1, तब p कक्षक होते हैं। फिर, Px या तो m=+1 या m=-1 है।
- बढ़ते n मानों के साथ, Px कक्षीय के बाहरी लोब का आकार धीरे-धीरे बढ़ता है जबकि आंतरिक लोब का आकार कम होता जाता है।
पाइ ऑर्बिटल क्या है?
Py कक्षक y-अक्ष के अनुदिश तीन p कक्षकों में से एक है। इस कक्षक में दो पालियाँ होती हैं। Py कक्षीय का क्वांटम अंकन इस प्रकार है।
- जब n=1, कोई P ऑर्बिटल्स नहीं होते हैं।
- जब n > 2, और l=1, तब p कक्षक होते हैं। फिर, Py या तो m=+1 या m=-1 है।
- बढ़ते हुए n मानों के साथ, Py कक्षक के बाहरी लोब का आकार धीरे-धीरे बढ़ता है जबकि आंतरिक लोब का आकार कम होता जाता है।
एक Pz कक्षीय क्या है?
Pz कक्षक z-अक्ष के अनुदिश तीन p कक्षकों में से एक है। इस कक्षीय में दो लोब होते हैं और एक डम्बल के आकार का होता है। Py कक्षीय का क्वांटम अंकन इस प्रकार है:
- जब n=1, कोई P ऑर्बिटल्स नहीं होते हैं।
- जब n > 2, और l=1, तब p कक्षक होते हैं। तब, Pz या तो m=0 है।
- बढ़ते n मानों के साथ, Pz कक्षक के बाहरी लोब का आकार धीरे-धीरे बढ़ता है जबकि आंतरिक लोब का आकार कम होता जाता है।
पीएक्स पाय और पीजेड ऑर्बिटल्स के बीच समानताएं क्या हैं?
- Px Py और Pz ऑर्बिटल्स का आकार एक जैसा (डम्बल शेप) होता है।
- सभी तीनों P ऑर्बिटल्स का आकार समान है।
- इन ऑर्बिटल्स के आकार n मान की वृद्धि के साथ बदलते हैं।
- सभी तीन कक्षकों में अक्ष के समान अभिविन्यास के साथ दो पालियाँ होती हैं।
पीएक्स पाय और पीजेड ऑर्बिटल्स में क्या अंतर है?
पीएक्स पीई बनाम पीजेड ऑर्बिटल्स |
||
| Px कक्षीय x-अक्ष के अनुदिश p कक्षीय उन्मुख है। | Py कक्षक y-अक्ष के अनुदिश p कक्षीय उन्मुख है। | Pz कक्षक z-अक्ष के अनुदिश p कक्षीय उन्मुख है। |
| ओरिएंटेशन | ||
| x-अक्ष के साथ | y-अक्ष के साथ | जेड-अक्ष के साथ |
| चुंबकीय क्वांटम संख्या का मान (एम) | ||
| चुंबकीय क्वांटम संख्या (एम) के लिए मान या तो +1 या -1 है। | चुंबकीय क्वांटम संख्या (एम) के लिए मान या तो +1 या -1 है | चुंबकीय क्वांटम संख्या (एम) के लिए मान 0 (शून्य) है |
सारांश – Px Py बनाम Pz ऑर्बिटल्स
एक परमाणु में तीन p परमाणु कक्षक होते हैं। Px, Py और Pz नाम अंतरिक्ष में कक्षीय के उन्मुखीकरण को इंगित करते हैं। Px Py और Pz ऑर्बिटल्स के बीच महत्वपूर्ण अंतर यह है कि Px ऑर्बिटल में x-अक्ष के साथ दो लोब उन्मुख होते हैं और Py ऑर्बिटल में y-अक्ष के साथ दो लोब उन्मुख होते हैं जबकि Pz ऑर्बिटल में z-अक्ष के साथ दो लोब उन्मुख होते हैं।